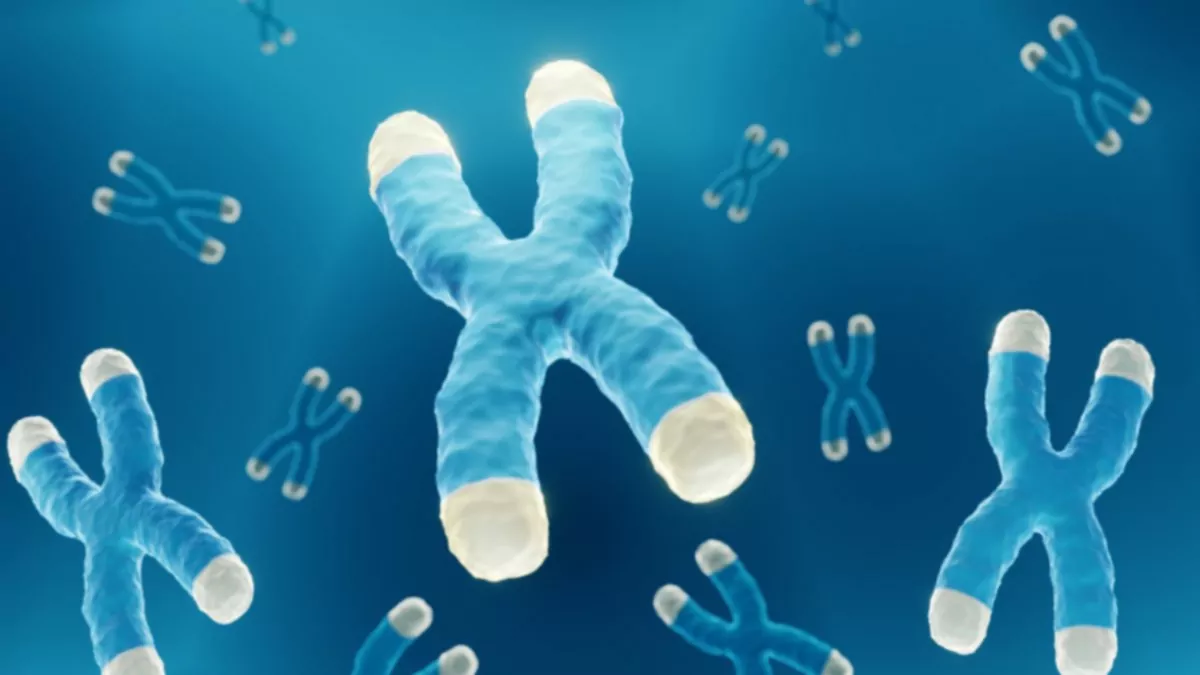
Telomery to "czapki", które chronią końce nici DNA przed zniszczeniem przez komórkę. Składają się one z obszarów powtarzających się sekwencji DNA połączonych ze specyficznymi białkami na końcach chromosomów — ciasno zwiniętych struktur DNA i białek wewnątrz komórek. Telomery odgrywają rolę w tym, jak szybko starzeją się komórki, choć dokładnie jak nie jest to całkowicie jasne.
Organizmy bez okrągłych chromosomów — w tym ludzie, inne zwierzęta, rośliny, a nawet jednokomórkowe protisty — mają telomery. Telomery działają jak bariery, zapobiegając degradacji i uszkodzeniu DNA.
Gdyby nasze komórki nie miały telomerów, maszyneria komórkowa "przegryzałaby końce chromosomów i istotne geny", powiedział Jan Karlseder (otwiera w nowej karcie) , profesor w Salk Institute for Biological Studies w Kalifornii i dyrektor Glenn Center for Biology of Aging Research w Salk Institute. Komórka może również dołączyć koniec jednego chromosomu do końca innego, co, jak powiedział, byłoby "katastrofalnym wydarzeniem" dla komórki.
"Ponieważ nasze chromosomy są liniowymi kawałkami DNA, rozwinęła się struktura zwana telomerem, która chroni naturalne końce chromosomów przed rozpoznaniem uszkodzenia DNA" - powiedział Karlseder w rozmowie z Live Science.
Przy każdym podziale komórki część powtarzającej się sekwencji w telomerach jest tracona. Kiedy telomery stają się zbyt krótkie, by efektywnie funkcjonować, komórka albo umiera, albo przestaje się dzielić. Ponieważ większość komórek nie potrafi regenerować swoich telomerów, z wiekiem stają się one coraz krótsze. Tempo skracania się telomerów zostało również powiązane z tempem starzenia się.
Jaką funkcję pełnią telomery?
U ludzi i wszystkich kręgowców, telomery powtarzają sekwencje nukleotydów TTAGGG — dwie cząsteczki tyminy, jedna adeniny i trzy guaniny. Nukleotydy to cząsteczki, które tworzą sekwencję DNA. U ludzi sekwencja ta może powtarzać się do około 3000 razy, ale liczba powtórzeń jest różna dla różnych gatunków. Na końcu telomerów znajduje się rodzaj "węzła" zwanego pętlą T, który jest utrzymywany przez specyficzną strukturę białkową zwaną kompleksem shelterin. Pętla T i shelterin utrudniają komórce niszczenie DNA na końcu chromosomu, natomiast powtarzające się sekwencje stanowią warstwy kodu genetycznego, które komórka może zniszczyć bez ingerencji w DNA potrzebne jej do funkcjonowania.
W większości komórek, telomery skracają się z czasem, gdy komórka niszczy więcej swojego kodu genetycznego. Jednak niektóre komórki, takie jak komórki macierzyste, które generują wiele typów wyspecjalizowanych komórek organizmu’oraz komórki germinalne, które tworzą jaja i spermę — mogą używać enzymu zwanego telomerazą do regeneracji swoich telomerów. Niektóre badania wskazują, że mogą istnieć sposoby na nieznaczne zwiększenie długości telomerów w innych typach komórek.
Telomery i starzenie się<<.
Większość komórek nie może zregenerować swoich telomerów, co powoduje ich skracanie się w ciągu życia zarówno komórki, jak i organizmu. "Skracanie telomerów naprawdę wyznacza długość życia naszych komórek, ograniczając liczbę podwojeń populacji lub proliferacji, którym komórki mogą się poddać" - powiedział Karlseder.
Od czasu nagrodzonej nagrodą Nobla pracy biolog Elizabeth Blackburn (otwiera się w nowej karcie) odkrywającej naturę telomerów i istnienie enzymu telomerazy, wiele badań wspiera związek między wiekiem biologicznym, długością telomerów, ogólnym stanem zdrowia i śmiertelnością.
Badanie z 2003 roku w czasopiśmie The Lancet (otwiera nową kartę) wykazało, że w próbie pozornie zdrowych osób w wieku powyżej 60 lat, które badacze śledzili przez dłuższy czas, osoby z krótszymi telomerami miały wyższy wskaźnik śmiertelności zarówno z powodu chorób serca, jak i chorób zakaźnych. W 2013 r. w pierwszym badaniu (otwiera się w nowej zakładce) tego rodzaju stwierdzono, że zmiany stylu życia w zakresie ćwiczeń, diety, radzenia sobie ze stresem i wsparcia społecznego były związane ze zwiększeniem długości telomerów w niewielkiej grupie mężczyzn z rakiem prostaty niskiego ryzyka. W przeglądzie z 2022 roku (otwiera się w nowej karcie) stwierdzono, że regularna umiarkowana lub energiczna aktywność fizyczna wydaje się pomagać w zachowaniu długości telomerów. Tempo skracania telomerów zostało powiązane z długością życia u różnych organizmów. Badanie z 2019 roku w czasopiśmie Proceedings of the National Academy of Sciences (otwiera się w nowej zakładce) wykazało, że podczas gdy ogólny pomiar długości telomerów organizmu nie miał żadnej korelacji z długością życia, to im szybciej telomery organizmu skracały swoją długość, tym krótsza była ich żywotność.

"Dokładne przyczyny starzenia się są nadal niezrozumiałe i nie jest jasne, dlaczego niektóre gatunki żyją krócej niż 1 [dzień], podczas gdy inne mogą żyć ponad 400 [lat]", czytamy w uderzającym otwarciu badania. Telomery mogą pomóc rzucić światło na tę długoletnią tajemnicę.
Badanie z 2021 roku opublikowane w czasopiśmie GeroScience (otwiera się w nowej karcie) zakłada, że konsekwencje długości telomerów mogą wpływać na to, jak stara jest dana osoba. Naukowcy przeanalizowali wyniki badań od ponad 400 000 uczestników UK Biobank, dużej bazy danych informacji o zdrowiu osób mieszkających w Wielkiej Brytanii. Odkryli, że ludzie, którzy mieli genetyczne predyktory dłuższej długości telomerów, częściej mówili, że ludzie mieli tendencję do myślenia, że wyglądają młodziej niż ich wiek.
- Powiązane: Czym są „niebieskie strefy” i czy naprawdę kryją sekret dłuższego życia?
Telomery i rak<<
Głównym sposobem powiązania telomerów ze zdrowiem jest ryzyko zachorowania na raka. Kiedy telomery stają się bardzo krótkie, DNA kopiowane podczas podziału komórek jest bardziej narażone na uszkodzenia, co może zwiększyć ryzyko zachorowania na raka.
Innym sposobem, w jaki nieprawidłowe działanie telomerów może prowadzić do raka, jest sytuacja, w której enzym telomeraza staje się aktywny w komórkach, w których nie powinien być.
"Całkiem sporo pojedynczych komórek nowotworowych znalazło mechanizmy pozwalające na utrzymanie telomerów i pokonanie ścieżki skracania telomerów" - powiedział Karlseder. "I to jest to, co utrzymuje komórki rakowe nieśmiertelne."
Organizm próbuje udaremnić raka, zapobiegając podziałom komórek ze zbyt krótkimi telomerami, co nazywane jest senescencją.
Karlseder, wraz z zespołem badaczy z Salk Institute, ukończył badanie, opublikowane w 2023 roku w czasopiśmie Nature (otwiera się w nowej karcie) , pokazując, jak telomery mogą wywołać śmierć komórki: Rozmawiają z mitochondriami komórki, jej dostawcą energii, aby wywołać śmiertelne zapalenie podczas kryzysu, inicjacji zaprogramowanej śmierci komórki w odpowiedzi na krytycznie krótkie telomery. Proces ten rzuca światło na to, jak telomery pomagają zapobiegać przekształcaniu się komórek w nowotwory.
Choć niektóre badania (otwiera w nowej karcie) sugerują, że ochrona, a nawet regeneracja, telomery mogą przedłużyć życie, Karlseder powiedział, że ryzyko wywołania raka czyni to dicey.
“Bardzo bym przestrzegał przed podejściami, które po prostu wydłużają telomery,” powiedział. “Wiemy, że doprowadzi to do raka, a niekoniecznie do długiego lifespan.”
Zamiast próbować przedłużyć długość życia i odwrócić starzenie, powiedział, naukowcy powinni być bardziej skoncentrowani na przedłużaniu "health span" — ilość czasu spędzonego w dobrym zdrowiu.
Jednym z celów procesu starzenia “naprawdę jest zapobieganie występowaniu raka" - powiedział Karlseder. "Powinniśmy powitać starzenie się jako mechanizm supresji nowotworów".